江苏国控电力设备有限公司
Jiangsu guo kong power equipment Co., Ltd.

2025年7月24日,中国国家药监局药品审评中心(CDE)官网显示,甲磺酸伏美替尼片的新适应证上市申请已正式申报,适用于既往经含铂化疗时或治疗后疾病进展、或不耐受含铂化疗,且经检测确认存在表皮生长因子受体20外显子插入突变(EGFR 20ins)的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
该适应症已于今年7月获CDE优先审评,并将进入附条件批准通道。这意味着,国内EGFR exon 20ins NSCLC治疗领域,即将形成“伏美替尼 vs 舒沃替尼 vs 安达替尼”三足鼎立的新格局。
1
破局之困
在肺癌治疗领域,EGFR 20外显子插入突变(EGFR ex20ins)一直被视为“难啃的硬骨头”。这种突变类型占所有EGFR突变非小细胞肺癌患者的10%左右,属于对常规靶向药物治疗不敏感、预后较差的亚型,按年新发2.5万例估算,国内存量患者超5万人。 长期以来,国内临床上一直缺乏针对这一突变类型的特效靶向药物。传统治疗方案效果有限,中位PFS仅3–5个月,患者预后普遍较差,存在巨大未满足需求。 艾力斯医药在2022年8月获得国家药监局临床试验批准后,加速推进伏美替尼针对EGFR ex20ins突变的临床研究 2 疗效突破 伏美替尼治疗EGFR ex20ins突变肺癌的疗效数据令人振奋。 在2023年世界肺癌大会(WCLC)上艾力斯公布了FAVOUR研究的初步结果,该研究共纳入358例局部晚期或转移性IIIB、IIIC或IV期不可切除非小细胞肺癌(NSCLC)患者,随机分为两组:178例接受伏美替尼治疗、180例接受吉非替尼治疗,结果显示: 在初治患者中,接受240mg伏美替尼治疗的客观缓解率(ORR)达到78.6%(22/28); 在经治患者中,240mg剂量组ORR为46.2%(12/26),160mg剂量组ORR也达到38.5%(10/26)。 伏美替尼组由独立评审委员会(IRC)评估的中位无进展生存期(PFS)显著延长至20.8个月(95%CI:17.8–23.5),而吉非替尼组仅为11.1个月(95%CI:9.7–12.5),风险比(HR)为0.44(95%CI:0.34–0.58,p<0.0001)。 特别值得一提的是,伏美替尼对脑转移患者显示出显著疗效。研究显示,有中枢神经系统转移患者的反应与无转移患者相似(ORR:33.3% vs. 40.6%),6个月无进展生存率达到69.4%。 3 3 市场格局:国产小分子“三国杀” 随着伏美替尼新适应症申报上市,国内EGFR ex20ins突变靶向治疗市场的竞争格局逐渐形成。 目前,针对这一适应症的国产药物仅有迪哲医药的舒沃哲®(舒沃替尼)于2023年8月获附条件批准上市。2025年7月3日,该药物获得美国FDA加速批准用于经治EGFR ex20ins突变NSCLC成人患者。 2025年5月22日,鞍石药业的EGFR抑制剂苯甲酸安达替尼胶囊新药上市申请也获CDE正式受理并纳入优先审评。 伏美替尼、舒沃替尼及安达替尼在国内EGFR ex20ins经治非小细胞肺癌领域即将形成“三足鼎立”之势。值得注意的是,这三个产品都获得了附条件批准,未来确证性临床试验结果将决定其市场地位。 随着伏美替尼新适应症的加速审批,中国EGFR ex20ins突变肺癌患者即将迎来新的治疗选择。全球多中心III期研究FURVENT/FURMO-004(NCT05607550)的推进,将决定这款国产创新药能否登上国际舞台。 除此之外,艾力斯还在积极推进伏美替尼的其他适应症研究,包括NSCLC EGFR敏感突变辅助治疗、PACC突变NSCLC一线治疗、EGFR敏感突变NSCLC伴脑转移患者治疗以及EGFR非经典突变辅助治疗等注册临床研究,如果您对是相关疾病的患者或者患者家属,欢迎关注"ai帮帮",了解更多临床资讯~ *声明:本文旨在科普肿瘤医学和新药进展,任何重大医疗决策请前往正规医疗机构就诊。 *版权申明:如需转载请联系小编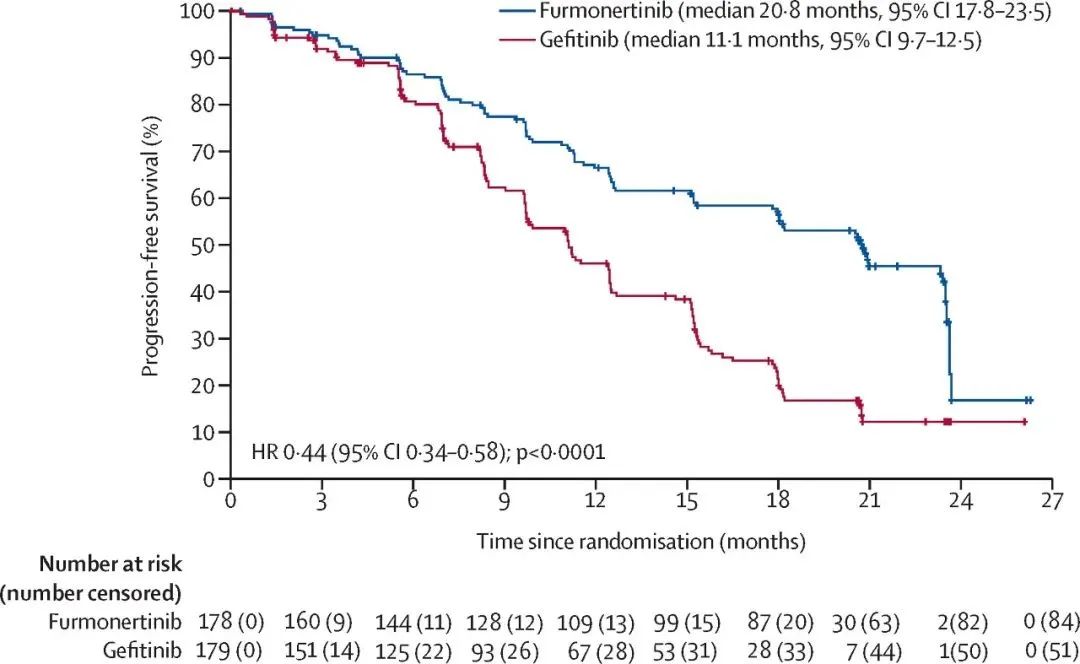

地址:上海市浦东新区康安路388弄1号T1栋


爱渡订阅号


爱渡服务号


邮箱:zixun@aibbang.com

爱渡小程序