江苏国控电力设备有限公司
Jiangsu guo kong power equipment Co., Ltd.

在 2025 年美国临床肿瘤学会(ASCO)年会上,Iza - bren(BL - B01D1)这一全球首创的靶向 EGFR×HER3 双特异性抗体药物偶联物(ADC)无疑是肺癌治疗领域的焦点。两项重磅研究(摘要号 3001 和 3002)分别聚焦非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),揭示了 Iza - bren 在肺癌治疗中的巨大潜力,为无靶向药可用的非经典突变NSCLC患者和免疫治疗失败的SCLC患者带来新的希望!
一.Iza-bren(BL-B01D1):双抗ADC的创新机制与全球突破
1.全球首创双抗ADC:设计理念与作用机制
lza - bren(BL - B01D1)是百利天恒全资子公司 SystImmune 和百时美施贵宝(BMS)共同开发的全球首创靶向 EGFR×HER3 的双特异性抗体药物偶联物(ADC)。其创新性在于同时靶向表皮生长因子受体(EGFR) 和 人表皮生长因子受体3(HER3) 两条关键信号通路。这种双靶点设计并非简单的叠加,而是基于对肿瘤信号网络交互作用的深刻理解:
抗体结构创新:采用双特异性抗体平台构建的抗体部分可同时结合EGFR和HER3,形成双靶点协同阻断效应。当抗体同时结合两个受体时,能诱导受体共内吞,显著提升药物内化效率。
连接子优化:采用四肽可切割连接子(Val-Cit linker),其在溶酶体中特异性裂解,确保毒素在肿瘤细胞内精准释放,减少系统性暴露。
载荷升级:偶联新型拓扑异构酶I抑制剂Ed-04,其细胞毒性是常用载荷依喜替康(exatecan)的3倍,且对多药耐药(MDR)表型肿瘤仍保持高效杀伤力。
这种设计赋予Iza-bren三重抗肿瘤机制:双重信号阻断(抑制EGFR/HER3介导的下游通路)、高效内化递送(提升肿瘤细胞内药物浓度)和强效旁观者效应(穿透肿瘤基质杀伤邻近细胞)。尤为重要的是,EGFR和HER3在包括SCLC、三阴性乳腺癌、头颈鳞癌等多种实体瘤中广泛共表达,使其具有广谱抗肿瘤潜力。
2.从实验室到全球舞台:研发历程与合作进展
Iza-bren的研发历程是中国创新药走向世界的缩影:
2023年首次人体(FIH)I期研究(NCT05194982)数据在《柳叶刀·肿瘤学》发布,显示其在多种实体瘤(包括EGFR野生型/突变型NSCLC、鼻咽癌、乳腺癌等)中的良好安全性和抗肿瘤活性(EGFR突变NSCLC队列ORR高达63.2%)。
2024年:美国百时美施贵宝(BMS)基于其突破性潜力,斥资81亿美元获得除中国区外的全球开发和商业化权益,创下中国生物制药License-out交易纪录。
2025年:两项关键I期研究(NSCLC与SCLC适应症)入选ASCO口头报告,由中山大学肿瘤防治中心杨云鹏教授与黄岩教授发布,引发全球关注。
目前,Iza-bren已在全球同步推进超过10项II/III期临床试验,覆盖NSCLC、SCLC、乳腺癌等多个适应症,其中针对SCLC的III期研究(NCT06500026)已完成首例患者入组。
二. Iza-bren (BL-B01D1)Yunpeng.Yang在伴有非经典EGFR突变驱动基因组改变 (GA) 的局部晚期或转移性非小细胞肺癌 (NSCLC) 患者中的一项I期研究(Yunpeng.Yang,3001)
研究背景:靶向非经典突变,弥补治疗空白
非小细胞肺癌(NSCLC)中存在多种驱动基因变异,除了经典 EGFR 突变外,还有 EGFR 20 号外显子插入突变、KRAS G12C 突变等多种基因异常。然而,针对这些非经典驱动基因变异的治疗选择十分有限,且疗效欠佳。Iza - bren 作为一种创新型 ADC 药物,通过同时靶向 EGFR 和 HER3,为这类患者提供了新的治疗可能。
研究方法:多队列扩展,精准给药
I 期 b 阶段研究涵盖了多个扩展队列,每个队列针对特定的基因变异,包括 EGFR 20 号外显子插入突变、非经典 EGFR 突变、HER2 突变、ALK、ROS1、BRAF(V600E 及其他)、KRAS(G12C 及其他)等。入组患者均为对标准靶向治疗耐药,且化疗线数不超过一线的患者。Iza - bren 的给药剂量为 2.5 mg/kg,在第 1 天和第 8 天静脉注射,每三周一次(Q3W)。
研究结果:高缓解率,良好安全性
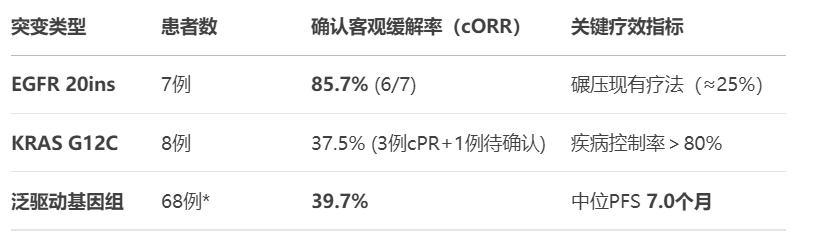
截至 2024 年 12 月 5 日,共入组 73 例伴驱动基因变异(GA)的 NSCLC 患者。在 7 例 EGFR 20 号外显子插入突变患者中,85.7%(6/7)达到确认的部分缓解(cPR);在 8 例 KRAS G12C 突变患者中,观察到 3 例 cPR 和 1 例待确认的 PR。
在安全性方面,最常见的血液学治疗相关不良事件(TRAEs)包括贫血(87.7%)、白细胞减少(74.0%)、血小板减少(74.0%)和中性粒细胞减少(72.6%);最常见的非血液学 TRAEs 为乏力(42.5%)、恶心(41.1%)、口腔炎(37.0%)、腹泻(32.9%)和脱发(31.5%)。3 级及以上不良事件主要为血液学毒性,但可通过标准支持治疗(如减量)有效管理,导致治疗中断的比例仅为 2.7%。仅观察到 1 例 2 级间质性肺病(ILD),未见与 Iza - bren 相关的死亡报告,也未发现新的安全性信号。
研究结论:开启精准治疗新方向
Iza - bren 在伴有非经典驱动基因变异的 NSCLC 患者中展现出良好的抗肿瘤活性及可控的安全性。这一成果不仅为非经典驱动基因变异 NSCLC 患者提供了新的治疗选择,也为未来精准医疗的发展开辟了新的方向。
三. 一项在局部晚期或转移性小细胞肺癌 (SCLC) 患者中开展的 Iza-bren (BL-B01D1)(一种 EGFR x HER3 双特异性抗体药物偶联物 [ADC])的 I 期研究(Yan.Huang,摘要号:3002)
研究背景:突破 SCLC 治疗困境
小细胞肺癌(SCLC)是一种侵袭性强、预后差的肺癌类型,传统治疗手段主要依赖化疗和放疗,但疗效有限。近年来,免疫治疗的应用为 SCLC 患者带来了一定的生存获益,但仍有很大的提升空间。Iza - bren 针对 EGFR 和 HER3 双通路的创新靶向机制,为 SCLC 治疗提供了新的思路。
研究方法:系统评估,探索最佳剂量
研究纳入了经治后进展的局部晚期或转移性 SCLC 患者,分别以 2.0、2.5 mg/kg 剂量在第 1、8 天给药(每 3 周一次,Q3W),或 4.5、5.0 mg/kg 剂量在第 1 天给药(Q3W)。每 6 周进行肿瘤扫描,评估疗效,尤其关注既往治疗暴露有限的患者。
研究结果:高缓解率,延长生存期
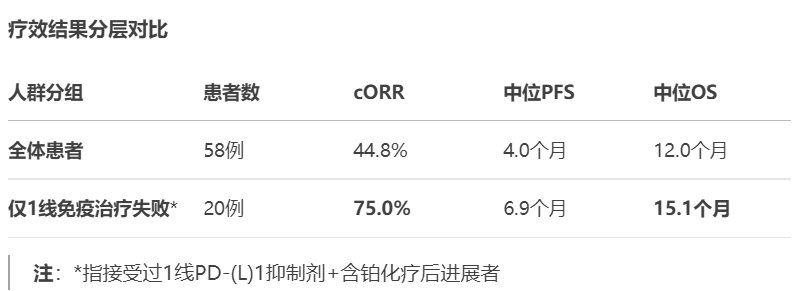
截至 2024 年 12 月 5 日,共纳入 58 例 SCLC 患者。中位随访时间为 16.4 个月,客观缓解率(ORR)为 55.2%,确认 ORR 为 44.8%,中位无进展生存期(PFS)为 4.0 个月,中位总生存期(OS)为 12.0 个月。在 2.5 mg/kg 剂量组的 52 例患者中,20 例仅接受过 1 线 PD - L1 与含铂化疗(PBC)联合治疗的亚组中,ORR 高达 80.0%,确认 ORR 为 75.0%,中位缓解持续时间(DOR)为 5.6 个月,中位 PFS 为 6.9 个月,中位 OS 达 15.1 个月。
在安全性方面,最常见的血液学 TRAEs(所有级别)为贫血(84.5%)、白细胞减少(74.1%)、血小板减少(72.4%)和中性粒细胞减少(70.7%);最常见的非血液学 TRAEs 为乏力(41.4%)、低白蛋白血症(39.7%)、口腔炎(34.5%)、恶心(31.0%)和呕吐(31.0%)。3 级及以上 TRAEs 以血液学为主,通过标准支持措施(包括剂量降低)可有效管理,治疗相关停药率为 12.1%。报告了 2 例与 Iza - bren 相关的感染性死亡(1 例呼吸衰竭,1 例胃肠道感染),未观察到间质性肺病(ILD),未发现新的安全信号。
研究结论:有望成为 SCLC 新型治疗选择
Iza - bren 在 SCLC 患者中显示出令人鼓舞的疗效和可控的安全性,特别是在既往治疗有限的患者中,高确认缓解率突显了其作为 SCLC 新型治疗选择的潜力。针对接受过 1 线 PD(L)- 1 与 PBC 联合治疗的 SCLC 患者的 Iza - bren III 期研究正在进行中,未来有望为 SCLC 患者提供更优质的治疗方案。
Iza-bren(BL-B01D1)作为全球首创的EGFR×HER3双抗ADC,在携带非经典驱动基因的NSCLC和SCLC中展现的卓越疗效,标志着难治性肺癌治疗范式的转变。其双靶点协同作用机制有效克服了肿瘤异质性和单靶点耐药,而高效载荷Ed-04则确保了强效的肿瘤杀伤能力。尤为重要的是,其对脑转移的控制潜力和可管理的安全性谱,为长期缺乏治疗选择的患者提供了新的生存希望。
目前,Iza-bren针对SCLC的全球III期研究(NCT06500026)及针对EGFR ex20ins的关键II期试验已全面启动。点击关注公众号”ai帮帮“,即刻匹配前沿临床试验
*声明:本文旨在科普肿瘤医学和新药进展,任何重大医疗决策请前往正规医疗机构就诊。
*版权申明:如需转载请联系小编
地址:上海市浦东新区康安路388弄1号T1栋


爱渡订阅号


爱渡服务号


邮箱:zixun@aibbang.com

爱渡小程序