江苏国控电力设备有限公司
Jiangsu guo kong power equipment Co., Ltd.

“癌症之王”——胰腺癌,长久以来都是医学界最棘手的难题之一。在美国,胰腺导管腺癌患者的5年生存率仅有3%,约80%的患者在确诊时已处于晚期或转移阶段,传统化疗的中位无进展生存期仅为2-3.5个月,临床急需创新疗法。
2025年6月,一则消息点燃了全球肿瘤学界的希望:美国FDA授予新药daraxonrasib(RMC-6236)突破性疗法认定,用于治疗携带KRAS G12突变的转移性胰腺导管腺癌患者。
更令人振奋的是,该药在临床试验中展现出惊人效果——接受治疗的KRAS G12X突变患者6个月生存率达到100%。
1
癌王的致命弱点
胰腺导管腺癌(PDAC)占所有胰腺癌病例的92%,是名副其实的“癌症之王”。其致命性源于两个关键因素:早期诊断困难,80%患者确诊时已属晚期;以及驱动其发展的核心机制——高达90%的PDAC患者携带RAS基因突变,其中约85%为KRAS G12突变。
RAS蛋白堪称癌症的“分子开关”。在正常细胞中,它控制着生长信号的通断;一旦发生突变,特别是G12、G13或Q61位点的突变,这个开关就被卡在“开启”位置,导致细胞无节制地增殖。高达 30% 的人类癌症由致癌 RAS 蛋白驱动,在 PDAC、非小细胞肺癌(NSCLC)和结直肠癌(CRC)中尤为显著。
几十年来,科学家们一直试图靶向这一靶点,但RAS蛋白表面光滑,缺乏传统小分子药物结合的“口袋”,使其成为著名的“不可成药”靶点
2
破局者的诞生
近期,美国 FDA 授予 Revolution Medicines 公司的 RAS(ON)多重选择性抑制剂 daraxonrasib(RMC - 6236)突破性疗法认定,用于治疗既往接受过治疗的、携带 KRAS G12 突变的转移性胰腺导管腺癌(PDAC)患者。

Daraxonrasib的问世标志着RAS靶向治疗进入新时代。与以往仅能靶向特定突变亚型(如KRAS G12C)的药物不同,它是一款口服的RAS(ON)多选择性抑制剂,能够同时靶向G12X、G13X和Q61X三种最常见致癌突变。
该药创新性地采用“分子胶”机制:通过与细胞内伴侣蛋白CypA结合,形成能“粘住”激活状态RAS蛋白的三元复合物,从而阻断RAS信号向下游传递。
此次认定主要基于 RMC - 6236 - 001 试验的积极数据。该试验是一项 1/1b 期多中心、开放标签、剂量递增和扩展研究,旨在评估 RMC - 6236 作为单药治疗携带 RAS 突变或野生型 RAS 晚期实体瘤患者的安全性、最佳剂量和疗效。截至 2024 年 9 月 30 日,共有 436 名患者入组。
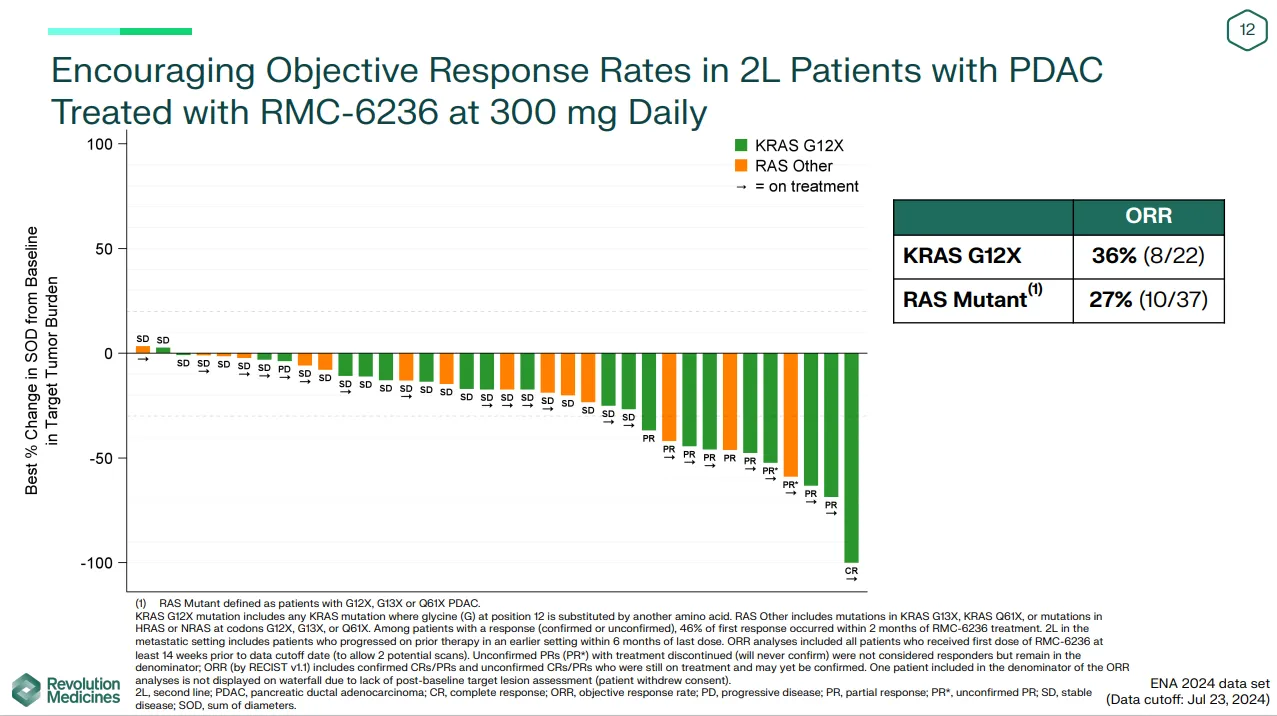
在 76 名携带 RAS 突变的 PDAC 患者中,每日一次 300 毫克剂量的 RMC - 6236 显示出良好的耐受性,其安全性与之前报告的数据一致,未观察到显著的安全信号差异。在 37 名携带 RAS 突变的 PDAC 患者中,RMC - 6236 作为二线疗法显示出显著的抗肿瘤活性:
KRAS G12X突变患者(n=22):中位无进展生存期(PFS)为8.8个月(95% CI:8.5个月–不可估计[NE]),中位总生存期(OS)仍不可估计(95% CI:NE–NE)。
任意RAS突变患者(n=37):中位PFS为8.5个月(95% CI:5.9个月–NE),中位OS仍不可估算(95% CI:8.5个月–NE)。
6个月生存率:KRAS G12X突变患者为100%,任意RAS突变患者为97%。
客观缓解率(ORR):KRAS G12X突变患者为36%,任意RAS突变患者为27%。
3
突破背后的战略布局
基于如此出色的早期数据,FDA于2025年6月授予daraxonrasib突破性疗法认定。这一认定旨在加速治疗严重疾病且满足未竟医疗需求的药物开发与审评。 几乎同时,Revolution Medicines宣布与Royalty Pharma达成一项高达20亿美元的合作协议,包括12.5亿美元的特许权使用费货币化和7.5亿美元的债务贷款。 这笔巨额融资为公司提供了充足弹药:推进正在进行的III期RASolute 302研究,并计划开展两项新的III期临床试验,评估daraxonrasib在一线治疗和辅助治疗胰腺导管癌的潜力。 当前III期RASolute 302研究正全球招募患者,设计聚焦于携带RAS G12X突变的核心人群,同时扩展至携带G13X或Q61X突变的患者。研究采用双重主要终点:核心患者的无进展生存期和总生存期。公司预计2025年基本完成入组,2026年获得关键数据。
4
未来战场:从单兵突进到联合围剿
尽管daraxonrasib单药已显示出显著疗效,但科学家们已在布局更广阔的前景。从全球研发管线看,胰腺癌治疗正呈现多条技术路线并进的局面。 分子胶技术路线以daraxonrasib为代表,其优势在于广谱抑制多种RAS突变。另一条路线是高选择性小分子抑制剂,如辉瑞的PF-07934040,其对KRAS的选择性比HRAS和NRAS高出5000倍,潜在安全性更佳。 在间接抑制RAS通路方面,Immuneering公司的双MEK抑制剂IMM-1-104崭露头角。其二期临床数据显示,联合化疗一线治疗胰腺癌的客观缓解率达43%,且几乎未增加额外毒性。 电场疗法也取得突破:Novocure/再鼎医药的TTFields联合化疗一线治疗胰腺癌的III期研究显示,中位总生存期达16.2个月,较单纯化疗延长2个月,且生存获益随时间增加,24个月生存率提高33%。 ADC药物(抗体药物偶联物)同样表现不俗:信达生物的CLDN18.2 ADC产品IBI343在43例二线及以上胰腺癌患者中,客观缓解率达32.6%,中位无进展生存期5.3个月;乐普生物的TF ADC产品MRG004A在12例患者中,客观缓解率33.3%,疾病控制率83.3%
III期RASolute 302研究预计将在2026年公布结果,如果数据积极,daraxonrasib有望成为首个获批用于RAS突变胰腺癌的广谱靶向药物。随着全球科研力量的汇聚,这将为胰腺癌治疗提供更多可能。
20亿美元的战略投资,近100%的六个月生存率,突破性疗法的加速通道——这些数字不仅代表科学突破,更是数十万胰腺癌患者更精准、有效的治疗选择。
欢迎关注"ai帮帮",了解更多临床资讯~
*声明:本文旨在科普肿瘤医学和新药进展,任何重大医疗决策请前往正规医疗机构就诊。 *版权申明:如需转载请联系小编
地址:上海市浦东新区康安路388弄1号T1栋


爱渡订阅号


爱渡服务号


邮箱:zixun@aibbang.com

爱渡小程序